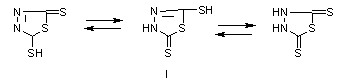ОРГАНИЧЕСКАЯ ХИМИЯ
УДК 542.91+632.938
Академик В.В. Довлатян, Т.З. Папоян, Ф.В. Аветисян, А.П.
Енгоян
Поиск новых пестицидов в ряду производных 1,3,4-тиадиазола
(Представлено 2/VI 2005)
Ключевые слова: гидразин,
пиримидин, тиадиазол, бис-алкилирование, фунгицид
В ходе поисков новых пестицидов нами ранее
было показано, что 2,4-дихлор-6-метилпиримидин под действием солей
диметилдитиокарбаминовой кислоты и 2-меркапто-4-метил-5-тиоксо-1,3,4-тиадиазола
в определенных условиях взаимодействия могут реагировать селективно,
исключительно по месту одного атома хлора, не затрагивая второго, что привело к
образованию 2-хлор-4-S-замещенных производных пиримидина [1,2].
В продолжение этих работ определенный интерес
представляло вовлечение в круг исследований более доступного
2-меркапто-5-тиоксо-1,3,4-тиадиазола, образующегося при взаимодействии гидрaзина
с сероуглеродом [3]. Соединение I может реагировать в нескольких таутомерных
формах:
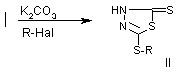
Однако под действием
алкилирующих средств в присутствии поташа I переходит в монозамещенные
производные II
|
|
R = C2H5 (a)
, CH2CONH2(б) ,
CH2-C6H4-Cl (в)
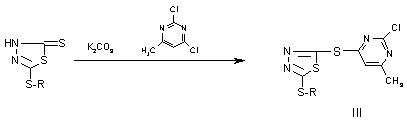
Взаимодействие полученных таким образом
соединений II с 2,4-дихлор-6-метилпиримидином привело к образованию соединений
III:
R = C2H5 (a) ,
CH2CONH2(б) , CH2-C6H4-Cl
(в)
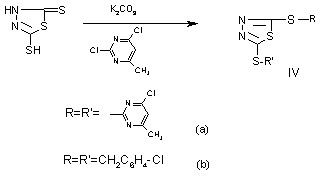
Одновременно было установлено, что соединение
I трудно и неоднозначно подвергается бис-алкилированию. Однако при применении в
качестве алкилирующих средств хлористого бензила и 2,4-дихлор-6-метилпиримидина
соединение I гладко поддается исчерпывающему алкилированию с образованием
бис-бензил (пиримидинил-4)-1,3,4-тиадиазолов:
|
|
По предварительным данным соединение IVа проявляет высокую фунгицидную
активность и может применяться в качестве протравителя семян озимой пшеницы
против твердой головни.
Спектры ЯМР ‘H сняты на спектрометре
"Mercury-300" с рабочей частотой 300 МГц. Чистота полученных веществ определена
методом ТСХ на пластинке "Silufol".
2-этилтио-5-тиоксо-1,3,4-тиадиазол(IIа). 0.28
г (0.002 моля) К2СО3 растворяют в 5 мл воды и добавляют
0.6 г (0.004 моля) 2-меркапто-5-тиоксо-1,3,4-тиадиазола. После полного
растворения при перемешивании и охлаждении прикапывают 0.63 г (0.004 моля)
С2Н5-J в 10 мл
ацетона. Перемешивание продолжают при температуре 50oС в течение 5 ч.
Оставляют на ночь. На следующий день растворитель упаривают при комнатной
температуре, остаток обрабатывают водой, отфильтровывают, высушивают. Получают
0.57 г (80%) II а. Т.пл. 126-127oС.
Найдено, %: N 15.55; S 53.50;
C4H6N2S3. Вычислено, %: N 15.73; S
53.93.
2-карбонамидометил-5-тиоксо-1,3,4-тиадиазол (II б). Получают
аналогич-но II а. Выход 84%. Т. пл. 185-186oС.
|
Соединение
|
Выход,
%
|
Т.пл.,0С
|
Найдено, % |
Брутто формула
|
Вычислено, % |
Спектр ПМР , б, ДМСО
–d6, м,.д |
|
N |
S |
Cl |
N |
S |
Cl |
|
III
а |
82 |
119-120 |
17.95 |
31.70 |
11.78 |
C9H9N4S3Cl |
18.39 |
31.53 |
11.66 |
1.50(3H,т,J=6.7
Гц
, CH3CH2S ); 2.50(3H,с,
CH3 ); 3.38(2H,к,J=6.7
Гц
, S CH2); 7.48(1H, c,
СH) |
|
Ш б |
83 |
164-165 |
20.85 |
29.05 |
10.91 |
C9H8N5ОS3Cl |
20.99 |
28.78 |
10.64 |
2.49(3H, c, СH3),4.08(2H,
c, СH2),7.45(1H,
c, СH),
7.10 и 7.55(по 1H,
уш.c,
NH2) |
|
Ш в |
80 |
109-110 |
14.15 |
24.22 |
17.33 |
C13H10N4S3Cl2 |
13.96 |
23.94 |
17.70 |
2.50(3H,
c,
СH3),4.58(2H,
c,
СH2),7.23-7.48(4H,
м,
С6H4),
7.47( 1H,
c,
CH) |
|
IVа |
82 |
194-195 |
20.58 |
24.15 |
17.46 |
C12H8N6S3Cl2 |
20.84 |
23.82 |
17.61 |
2.51[6H,c,(CH3)2],
7.55[2H,c,(CH)2 |
|
|
Найдено, %: N 19.97; S 47.00;
C4H5N3S3O. Вычислено, %: N 20.29; S
46.37.
2-п-хлорбензил-5-тиоксо-1,3,4-тиадиазол (II
в). Получают аналогично II а. Выход 82%. Т. пл. 240-242oС.
Найдено, %: N 10.55; S 34.25; Cl 12.80;
C9H7N2S3Cl. Вычислено, %: N 10.20; S
34.97; Cl 12.93.
2-хлор-4-(2’-этилтио-1,3,4-тиадиазолил-5’)-тио-6-метилпиримидин (III а).
1.78 г (0.01 моля) II а растворяют в 10 мл воды, добавляют при перемешивании
0.69 г (0.005 моля) К2СО3. После полного растворения при
охлаждении и перемешивании прикапывают 1.63 г (0.01 моля)
2,4-дихлор-6-метилпиримидина в 10 мл ацетона. Смесь при перемешивании нагревают
при 50oС в течение 5 ч, оставляют на ночь. На следующий день
растворитель упаривают при комнатной температуре, обрабатывают водой,
отфильтровывают. Очищают кипячением в гексане и отфильтровыванием в горячем
состоянии. Получают 2.5 г III а (таблица).
2-хлор-4-(2’-карбонамидометилтио-(III б) и
2-хлор-4-(2’-п-хлорбензилтио-1,3,4-тиадиазолил-5’)-тио-6-метилпиримидин (III в).
Получают аналогично III а (таблица).
2,5-бис-(2’-хлор-6’-метилпиримидинил)-5-тио-1,3,4-тиадиазол (IV а). 1.38
г (0.01 моля) К2СО3 растворяют в 10 мл воды и при
перемешивании добавляют 1.5 г (0.01 моля)I. К полученному раствору при
охлаждении льдом и перемешивании добавляют 3.26 г (0.02 моля)
2,4-дихлор-6-метилпиримидина в 10 мл ацетона. Перемешивание продолжают при
температуре 50oС в течение 5 ч, оставляют на ночь. На следующий день
растворитель упаривают при комнатной температуре, обрабатывают водой,
отфильтровывают. Очищают кипячением в гексане и отфильтровыванием в горячем
состоянии. Получают 3.3 г IV а (таблица).
2,5-бис-(п-хлорбензил)-5-тио-1,3,4-тиадиазол
(IV б). Получают аналогично IV а. Выход 93%. Т.пл. 230-231oС.
Найдено, %: N 6.84; S 24.22; Cl 18.30;
C16H12N2S3Cl2. Вычислено,
%: N 7.01; S 24.06; Cl 17.79.
Государственный аграрный университет
Армении
Литература
1. Довлатян В.В., Папоян Т.З.,
Аветисян Ф.В., Енгоян А.П. - ДНАН Армении. 2004. Т.104. N3.
С. 202-206.
2. Патент РА, №
1540,2004.
3. Busch. - B. 1894. V. 27. P. 2518.