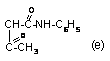|
|
|
|
|
R=CH3(a),
CH2COOH (б),
CH2COOC2H5 (в),
CH2CONH2 (г),
CH2C≡N (д), |
|
|
Взаимодействием хлористого триметил-4,6-бис-изопропиламино-симм-триазинил-2-аммония с I получен 2-(2'-тио-4'-метил-5-тиоксо-1,3,4-тиадиазолил-2')-4,6-бис-изопропиламино-симм-триазин IV.
|
|
Соединение III под действием триметиламина в
среде бензола образует ожидаемую четвертичную аммониевую соль V.
Благодаря высокой реакционной способности
соединение V легко реагирует с нуклеофилами, что было показано на примере
получения его роданпроизводного VI.
Соединения III, V, VI, представляющие
самостоятельный интерес в качестве пестицидов, могут успешно применяться для
целенаправленной функционализации пиримидина. ИК и ЯМР 'H спектры сняты на
приборах "Specord IR-75" в вазелиновом масле и "Varian T-60". Чистота полученных
веществ определена методом ТСХ на пластинке "Silufol".
Соединение Выход, Т. пл.,
Найдено,%
Брутто
Вычислено,% Спектр ЯМР 'H,
δ, м.д.
N
S N
S
IIa
79
88-89
15.50
53.26
C4H6N2S
15.73
53.93
2.65(3H, c, SCH3);
IIб
81
98-100
12.30
42.75
C5H6N2O2S3
12.20
43.40
IIв
78
60-61
11.49
37.89
C7H10N2O2S3
11.25
38.40
IIг
80
120-121
19.17
43.00
C5H7N3OS3
19.23
43.44
IIд
89
124-125
20.82
46.85
C5H5N3S3
20.69
47.29
3.83(3H, c, NCH3);
IIе
82
140-142
12.56
29.00
C13H13N3O2S3
12.39
28.32
1. Мельников Н. Н. Пестициды. Химия, технология и применение. М. Химия. 1987. C.
612-616.


..
3.75(3H, c, NCH3);
3.80(3H, c, NCH3);
4.11(2H, c, SCH2);
3.82(3H, c, NCH3);
2.38(3H, c, CH3);
Армянская сельскохозяйственная академия
2. Справочник по пестицидам. М. Химия. 1985.
3. Довлатян В. В., Джаванширян Т. Л., Аветисян Ф. В.,
Енгоян А. П. - Химический журнал Армении, в печати.