УДК 597.82:612.886
Пространственное распределение нейронов вестибулярных
ядер,
проецирующихся к различным сегментам спинного мозга лягушки
(Представлено 6/VI 2001)
Двигательные структуры у бесхвостых подвержены значительной модификации в связи с изменением среды их обитания (частичный или полный переход на сушу) и с развитием четырехконечностного тела [1-3]. Нахождение бесхвостых на раннем этапе эволюционного развития определяет наименьшую дифференциацию их вестибуломозжечковых областей по сравнению с другими четвероногими [4]. На этом этапе вестибулярный ядерный комплекс (ВЯК) уже представляет центральную структуру, оказывающую регулирующее влияние на моторные центры [5,6]. Устройство и топография индивидуальных ядер в ВЯК у бесхвостых и млекопитающих имеют много общих черт. У лягушки также выделены верхнее (ВВЯ), латеральное (ЛВЯ), нисходящее (НВЯ) и медиальное (МВЯ) вестибулярные ядра [7-9]. Вестибулоспинальный тракт у лягушки представляет выраженную нисходящую систему спинного мозга. Он в основном нисходит ипсилатерально [7]. Частичный перекрест волокон происходит на уровне продолговатого и спинного мозга [4]. Мало известно об особенностях пространственной организации эфферентных нейронов, дающих начало вестибулоспинальным волокнам. На жабах Bufo bufo L. с использованием ретроградного аксонного транспорта пероксидазы хрена (ПХ) [10] установлено,что в пределах вентрального вестибулярного ядра рострально расположенные клетки, главным образом сконцентрированные в дорсомедиальной позиции, проецируются в шейный отдел спинного мозга; каудально расположенные клетки с преимущественной локализацией в вентролатеральной части проецируются к более нижним сегментам спинного мозга. На основании вышеотмеченного было сделано заключение, что у жаб имеется соматотопическая организация вестибулоспинальной проекции. В других морфологических работах, выполненных на бесхвостых, сообщались лишь фрагментарные сведения о пространственном распределении нейронов, являющихся источниками вестибулоспинальных волокон [8,11].
|
|
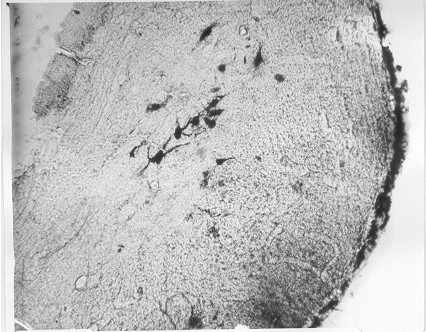
Микрофотография меченых нейронов и волокон в вестибулярном
ядерном
комплексе лягушки в результате микроионофоретического введения
пероксидазы хрена в спинной мозг. Увеличение: об. 10 х, ок. 8 х.
Целью настоящей работы было
посредством локальных микроионофоретических инъекций пероксидазы хрена в
различные отделы спинного мозга лягушки подробно исследовать траектории
ретроградно меченных ферментом волоконных систем и топографию распределения в
ВЯК нейронов - источников вестибулоспинальных волокон.
2
3 Т
нейроны
Общее число нейронов
44
34
71 Латеральное
вестибулярное ядро
21
26
53
4
7
14
Средняя
часть
3
3
11
Каудальная
часть
14
16
28
12
12
26
9
14
27
Нисходящее
вестибулярное ядро
19
8
18
15
1
7
Средняя
часть
2
1
1
Каудальная
часть
2
6
10
9
1
7
10
7
11
Медиальное
вестибулярное ядро
4
0
0
3
0
0
Средняя
часть
0
0
0
Каудальная
часть
1
0
0
1
0
0
3
0
0
2
3 Т
нейроны
Общее число нейронов
16
3
15 Латеральное
вестибулярное ядро
12
1
8
1 1
0
Средняя
часть
0
0
2
Каудальная
часть
11
0
6
2
0
5
10
1
3
Нисходящее
вестибулярное ядро
4
2
4
2
1
0
Средняя
часть
1
0
0
Каудальная
часть
1
1
4
2
1
1
2
1
3
Медиальное
вестибулярное ядро
0
0
3
0
0
0
Средняя
часть
0
0
0
Каудальная
часть
0
0
3
0
0
1
0
0
2 ядре клеток, меченных ПХ, в целом затрудняет сколько-нибудь
обоснованный вывод в пользу его соматотопической организации. В МВЯ было
обнаружено только несколько С нейронов. Институт физиологии им Л.А.Орбели НАН РА
1. Larsell O. The Comparative Anatomy and Histology of the Cerebellum from Myxinoids
through Birds. Minneapolis. University of Minnesota Press.
1967.
Таблица 1
Количественное распределение С, Т
и L вестибулоспинальных нейронов в
вестибулярных ядрах при лягушек при введении энзима в ипсилатеральную половину
шейного (лягушка №1), грудного
(лягушка №2) и поясничного
(лягушка №3)
отделов спинного мозга
Лягушка
№
1
Вестибулоспинальные
нейроны
С
нейроны
L
нейроны
Ростральная часть
Дорсальная половина
Вентральная
половина
Ростральная часть
Дорсальная половина
Вентральная
половина
Ростральная часть
Дорсальная половина
Вентральная
половина
Таблица
2
Количественное распределение С, Т
и L вестибулоспинальных нейронов в
вестибулярных ядрах тех же лягушек, что и в табл. 1, при введении энзима в
контралатеральную половину шейного (лягушка №1), грудного
(лягушка №2) и
поясничного
(лягушка №3) отделов спинного мозга
Лягушка
№
1
Вестибулоспинальные
нейроны
С
нейроны
L
нейроны
Ростральная часть
Дорсальная половина
Вентральная
половина
Ростральная часть
Дорсальная половина
Вентральная
половина
Ростральная часть
Дорсальная половина
Вентральная
половина
2. Montgomery N.M.
- Brain Behav. Evol. 1988.V. 31. P.
82-95.
3. Ten-Donkelaar H.J., De
Boer-Van Huizen R., Schouten F.T.M., Eggen S.J.H. -
Neuroscience. 1981. V.6. P. 2297-2312.
4. Kappers A.C.U., Huber G.C., Grosby E.C. The
comparative anatomy of the nervous system of vertebrates, including man. V.1, N.
Y. Hafner Publ.Comp. 1960.
5. Maeda M., Magherini P.C., Precht W. - J.
Neurophysiol. 1977. V.40. P. 225-244.
6. Magherini P.C., Precht W., Richter A. - Pflugers
Arch. 1974.V.348.P. 211-223.
7. Fuller P.M. - Brain Behav. Evol. 1974. V.10.
P.157-169.
8. Kuruvilla A., Sitko
S., Schwartz I.R., Honrubia V. - Laryngoscope.1985.V. 95. P.
692-707.
9. Matesz C. - Neuroscience 1979. V.4.
P.2061-2071.
10. D'Ascanio P.,
Corvaja N. - Arch. ital. Biol. 1981. V.119. P.
139-150.
11. Ten Donkellar H.J.
Anurans In: The Central Nervous System of Vertebrates.Eds.
R.Nieuwenhuys, H.J. Ten Donkellar, C. Nicholson. Springer.1997. V. 2.
P.1151-1314.
12. Mesulam M.M.
- J. Histochem. and Cytochem. 1978. V.26.
P.106-117.
13. Fanardjian V.V.,
Manvelyan l.R., Zakarian V.L., Pogossian V.I., Nasoyan A.M. - Neuroscience. 1999,V. 94, P.
845-857.
14. Fanardjian V.V.,
Manvelyan L.R., Nasoyan A.M. - Neuroscience. 2001. V.104.
P.853-862.