ФИЗИЧЕСКАЯ ХИМИЯ
УДК 541.095
А. А. Мхитарян
Энергетика взрывных реакций на наковальнях
Бриджмена
Представлено академиком К. А. Костаняном 14/XII 2000)
В работах [1-5] показано, что в условиях
взрыва на наковальнях Бриджмена инициируются многие твердофазные экзотермические
реакции, протекающие с детонационной скоростью. При осуществлении
сильноэкзотермических безгазовых реакций, типа металлотермических, нередко
наблюдались бурные превращения, часто приводящие к разрушению наковален
[4]. Между тем при осуществлении реакций, сопровождающихся образованием
газообразных продуктов, разрушительных эффектов не наблюдали. Все это не
согласуется с общепринятой теорией детонации конденсированных систем [6],
требующей для формирования ударной волны наличия газовой фазы.
Для обстоятельного изучения вопроса и
выявления причин, приводящих к разрушительным эффектам, была поставлена серия
экспериментов. Взрывные химические реакции осуществляли на установке
высокого давления типа наковален Бриджмена, подробное описание которой и
методика работы приводятся в [1-5]. Объектами исследования были выбраны
термитные реакции восстановления некоторых оксидов различными
металлами. Эти смеси составлялись в соответствии с их
стехиометрией. Кроме этого изучалось поведение бихромата аммония и
аммиачной селитры, в отличие от термитных реакций разлагающихся в условиях
взрыва с образованием газообразных продуктов.
Было установлено, что разрушительные эффекты (бризантность) термитов
зависят от экзотермичности реакций и от массы взрываемой таблетки.
В табл. 1 приведены данные о тепловых
эффектах Q, изменениях объема твердой фазы реагирующей смеси \triangle Vтв. Определены критические массы термитов mкр, приводящие к разрушениям и
соответствующие им пороги энергии Eкр.
Как видим, порогом энергии Eкр, вызывающим катастрофические эффекты (разрушение), является
2,3ё2,5 кДж. Дополнительные опыты, проведенные с
другими оксидами (Cu2O, FeO, Fe2O3 и др.), а
также с трехкомпонентными смесями (два металла +CuO) убедили нас в том, что
разрушения наблюдаются именно в указанном интервале пороговой
энергии. Таким образом, для безгазовых (термитных) реакций масса взрываемой
таблетки является ограниченной. Наиболее опасными являются три первых
термита (табл. 1), имеющих высокий тепловой эффект на единицу массы и,
следовательно, низкие значения критических масс.
Таблица 1
Некоторые свойства и бризантность различных термитов
|
|
Q, кДж |
ΔVтв, см3 |
|
|
| № |
Термитная реакция |
на 1 моль |
на 1 г |
на 1 моль |
на 1 г |
mкр, |
Eкр, |
|
|
CuO |
смеси |
CuO |
смеси |
г |
кДж |
|
|
| 1 |
Mg+CuO ® MgO+Cu |
440 |
4.23 |
-8.0 |
-7.7·10-2 |
0.6 |
2.5 |
| 2 |
2Al+3CuO ®
Al2O3+3CuO |
396 |
4.0 |
-3.3 |
-3.4·10-2 |
0.6 |
2.4 |
| 3 |
Si+2CuO ® SiO2+2Cu
|
294 |
3.2 |
0 |
0 |
0.7 |
2.3 |
| 4 |
Zn+CuO ® ZnO+Cu |
89 |
1.3 |
-0.2 |
-0.14·10-2 |
1.8 |
2.3 |
| 5 |
Sn+CuO ® SnO+Cu |
124 |
0.8 |
-1.9 |
-0.1·10-2 |
3.8 |
2.4 |
| 6 |
Fe+CuO ® FeO+Cu |
103 |
0.76 |
0.3 |
0.22·10-2 |
3.0 |
2.3 |
| 7 |
Pb+CuO ® PbO+Cu |
57 |
0.2 |
0 |
0 |
* |
-
|
* Разрушений не наблюдали
Совершенно иначе ведут себя в
подобных условиях бихромат аммония (БА) и аммиачная селитра (АС), разлагающиеся
в условиях взрыва по уравнениям:
|
| (NH4)2Cr2O7 ®
Cr2O3 + N2 + 4H2O
;
NH4NO3 ®
0.75N2 + 0.5NO2 + 2H2O ;
| |
| (Q = 300 кДж/моль = 1.2 кДж/г ;
(Q = 100
кДж/моль = 1,25 кДж/г ; | |
| ΔVтв = -87
см3/моль = -0,35 см3/г)
; ΔVтв = -46.4
см3/моль = -0,58 см3/г)
. | | |
| |
Несмотря на то, что эти реакции являются достаточно экзотермичными, их
взрывные превращения никогда не приводят к разрушительным эффектам, хотя и около
2 г этих веществ
достаточно для выделения энергии в пределах 2,4-2,5
кДж, приводящей к катастрофическим эффектам, как это происходит при безгазовых
превращениях термитов. Следовательно, газообразные продукты как бы смягчают
бризантные свойства реагентов.
Для
дополнительной проверки смягчающего действия газовой фазы нами были составлены
смеси аммиачной селитры с кремниево-медным термитом. Последний удобен в том
отношении, что при реагировании не дает усадки таблетки (табл. 1), и
поэтому изменение объема твердой фазы смеси термит +АC будет зависеть только от
содержания аммиачной селитры.
В табл. 2 приведены результаты опытов по определению
бризантных свойств указанных смесей с различным массовым содержанием
составляющих.
Как видим, начиная
приблизительно с 60% содержания аммиачной селитры взрывы становятся
"безопасными". Аналогичные данные получены при замене аммиачной селитры на
бихромат аммония, когда около 80% добавки БА приводит к предотвращению
разрушительных эффектов.
Таблица 2
Бризантные свойства смеси кремниево-медный термит +
AC
|
Массовый % |
Расчетные данные на 1 г
смеси |
|
|
| № |
Si + 2CuO, |
NH4NO3, |
Q, |
mгаз, |
ΔVтв,
|
mкр, |
Eкр, |
|
термит |
AC |
кДж |
г |
см3 |
г |
кДж |
|
|
| 1 |
100 |
0 |
3.2 |
0 |
0 |
0.7 |
2.3 |
| 2 |
80 |
20 |
2.81 |
0.2 |
-0.0116 |
1.2 |
3.4 |
| 3 |
60 |
40 |
2.42 |
0.4 |
-0.232 |
3.5 |
8.5 |
| 4 |
40 |
60 |
2.03 |
0.6 |
-0.348 |
12.0 |
24.4 |
| 5 |
20 |
80 |
1.64 |
0.8 |
-0.464 |
- |
- |
| 6 |
0 |
100 |
1.25 |
1.0 |
-0.58 |
- |
-
|
Для объяснения экспериментальных фактов нами
выдвинуто предположение [5], что при взрывных превращениях на наковальнях
Бриджмена осуществляется так называемая низкотемпературная твердофазная
детонация, движущей силой которой является упругая волна. Энергия
химической реакции непосредственно переходит в механическую в виде упругих
напряжений, которые вызывают распространение энергии в системе упругой
волной. Экзотермический процесс поддерживает распространение упругой волны,
не давая ей затухать, что и приводит к самораспространению детонационного
превращения в объеме исследуемой таблетки. При этом наличие или отсутствие
газов в системе не играет определяющей роли для поддержания волнового
процесса. Упругая волна, осуществляя реакцию, переносит избыток энергии со
скоростью звука по всей системе и поглощается установкой высокого давления
(наковальни, пресс). Поскольку масса установки по сравнению с массой
исследуемого вещества огромна, то установка играет роль термостата и ее
температура практически не меняется. При этом если энергия, переносимая
упругой волной, достаточна для возбуждения интенсивного колебательного процесса
в наковальнях, превосходящего предел их прочности, то последние
разрушаются. Понятно, что при такой форме передачи энергии важную роль
играет сплошность среды. Поэтому смягчающее действие газообразных продуктов
объясняется тем, что твердофазный контакт продуктов реакций от наковален как бы
теряется, что и предотвращает разрушительные эффекты; кроме того часть
механической энергии затрачивается на работу вывода газообразных продуктов из
зоны реакции и сообщения им кинетической энергии вылета.
Понятно, что часть упругих напряжений успеет
отрелаксироватъ с превращением в тепло, разогревающее систему. Поэтому
баланс химической энергии можно представить в виде Qx.p=Qт+Eynp, где Qт - энергия, идущая на нагрев системы, Eупр
- энергия, переходящая в упругие напряжения. Возникает вопрос - каково
соотношение между Qт и Eупр?
Произведем ориентировочные расчеты для
бихромата аммония в предположении, что взрывное превращение осуществляется для 1
моль БА (252г). Из уравнения реакции находим Qх.р=300
кДж/моль, ΔVтв=-87 см3/моль, масса
газообразных продуктов составляет 100 г.
Из
общеизвестной формулы Qт=(n1CCr2O3+n2CH2O+n3CN2)ΔT, где n - число молей продуктов реакций, C - их теплоемкость, можно
найти энергию реакции, идущей на нагрев системы. Теплоемкость продуктов
реакции составляет [8] C(Cr2O3)=118.8 Дж/моль K,
C(H2Oгаз)=33.58 Дж/моль K,
C(N2)=29.1 Дж/моль K.
В работе
[7] показано, что температура продуктов реакции не может превышать
100oС, следовательно, максимальное повышение температуры по сравнению
с комнатной не превысит 80oС, что дает повод заключить, что Eупр >> Qт, т. е. основная
часть химической энергии непосредственно переходит в механическую.
Принимая ΔT=80 K, находим Qт » 23 кДж/моль,
т. е. основная часть химической энергии выделяется не по тепловому
механизму, а переходит в энергию упругих напряжений Eупр. Работу вывода газообразных продуктов можно рассчитать
по формуле A=PV [9], где P - давление в системе,
V - объем выведенного газообразного элемента. Учитывая, что
критические давления взрыва в наших опытах в среднем составляли 10 кбар, а объем
выведенного элемента V=ΔVтв=87cм3, и
используя соотношение 1л атм=0,1 кДж, легко показать, что
ΔVтв (в см3) численно равна работе, выраженной в
кДж. Для бихромата аммония она составляет 87 кДж/моль. Таким образом в
избытке остается около 19 кДж энергии. Используя формулу для кинетической
энергии Eкин =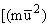 /2], можно рассчитать среднюю скорость вылета
/2], можно рассчитать среднюю скорость вылета
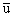 газообразных молекул из зоны реакции. Учитывая,
что mгаз=100 г=0.1 кг, получим
газообразных молекул из зоны реакции. Учитывая,
что mгаз=100 г=0.1 кг, получим
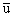 » 2000 м/с, что хорошо
согласуется с данными автора [10].
» 2000 м/с, что хорошо
согласуется с данными автора [10].
В работе
[7] показано, что скорость фронта химической реакции БА составляет 1.3±0.2 км/с, что объясняет, почему в системе не формируется
ударная волна. Действительно, для формирования ударной волны в системе
скорость фронта реакции (газоприход) должна превышать скорость вылета
газообразных частиц (газоотвод), между тем в наших условиях наблюдается обратная
закономерность.
Таким образом, смягчающее
действие газообразных продуктов при упруговолновом механизме передачи энергии
объясняется несколькими факторами: часть энергии химических реакций
затрачивается на работу вывода газообразных продуктов и на сообщение им
кинетической энергии вылета из зоны реакции, при этом начиная с некоторого
порога усадки таблетки как бы теряется "твердофазный контакт" продуктов реакции
с металлическими частями установки; кроме тогo в системе не реализуются условия
для образования ударной волны, что в совокупности и приводит к предотвращению
разрушительных эффектов.
Армянская сельскохозяйственная
академия
Литература
1. Ениколопян H. C.,
Мхитарян А. А., Карагезян А. С. - ДАН СССР. 1986.
Т. 288. № 3. С. 657-660.
2. Ениколопян H. C., Мхитарян А. А., Карагезян А. С.,
Хзарджян С. М. - ДАН СССР. 1986. Т. 288, № 4. С.
911-914.
3. Ениколопян
H. C., Мхитарян А. А., Карагезян А. С., Хзарджян А. А.
- ДАН СССР. 1987. T. 292. № 4. С. 887-890.
4. Ениколопян H. C.,
Мхитарян А. А., Карагезян А. С. - ДАН СССР. 1987.
Т. 294. № 4, С. 912-915.
5. Ениколопян H. C., Мхитарян А. А. - ДАН
СССР. 1989. Т. 309. № 2. С. 384-387.
6.
Андреев К. К., Беляев А. Ф. Теория взрывчатых
веществ. М.: Оборонгиз, 1960. 595 с.
7.
Мхитарян А. А. - Агронаука. 2000. 7-8. (№
505-506). С. 366-370.
8. Свойства неорганических соединений. Справочник. Л.: Химия, 1983.
390 с.
9. Исаев С. И.
Курс химической термодинамики. М.: Машиностроение,
1975. 256 с.
10. Ярославский М.
А. Реологический взрыв. M.: Наука, 1982. 193 с.